2025年终,本实验室周竑钊研究员收到《Nature Methods》编辑Michelle Korda博士的一封信,对他们于2025年发表于《Science Advances》的“3D bioprinted human-scale intestine models for physiological and microbial insights through fluid-driven heterogeneity”研究文章产生了极大兴趣,并针对研究内容询问了若干问题。随后该刊在2026年第1期“研究热点(Research Highlight)”栏目以“生物打印人体小肠(Bioprinting a human small intestine)”为题对这篇研究论文进行了专题报道。
Nature Methods编辑点评了这项研究的亮点:沈璐琦,周竑钊报道了一种生物3D打印的人体尺度肠道模型,该模型内衬上皮细胞,能够重现生理相关的结构以及力学和功能相互作用,量化药物吸收和宿主-微生物相互作用, 实现了同一系统中结构、力学环境与功能行为的协同再现。

Science Advances发表的研究成果之所以吸引了Nature Methods专业编辑的关注,源于浙江大学流体动力基础件与机电系统全国重点实验室杨华勇院士团队周竑钊课题组攻克了一项长期被忽视却始终难以突破的工程难题:即如何在体外系统中,同时实现“足够大、足够真、还能稳定工作”的人体小肠模型。

真实小肠并非一段简单的直管,而是具有连续弯曲和褶皱结构的大尺度器官,这些结构会自然塑造内部液体流动方式,并进一步决定细胞功能分区和微生物定植行为。现有的体外人工小肠模型要么尺度过小、结构过于理想化,要么难以长期维持稳定运行,导致结构、流动与功能之间的关系无法被系统研究。因此,如何在体外系统中准确重建小肠复杂的生理调控机制,一直是生物医学工程领域的核心挑战之一。
针对这一瓶颈,本研究从工程设计的角度出发,创新性地构建了一种基于三维生物打印的体外仿生小肠组织模型。通过设计并制造具有仿生环形襞结构、接近人体尺度的小肠构型,模型在持续灌流条件下能够自发形成区域特异性的力学微环境,并进一步主导肠上皮功能的空间分化,体外重建“结构决定流动、流动塑造功能”的自然过程,实现了小肠模型从“形态相似”向“功能相符”的关键跨越。相关成果以“3D bioprinted human-scale intestine models for physiological and microbial insights through fluid-driven heterogeneity”为题发表于《Science Advances》。论文第一作者为浙江大学博士生高梓祺与杜慧龙,通讯作者为浙江大学周竑钊研究员与西湖大学沈璐琦助理研究员。第一完成单位为流体动力基础件与机电系统全国重点实验室。
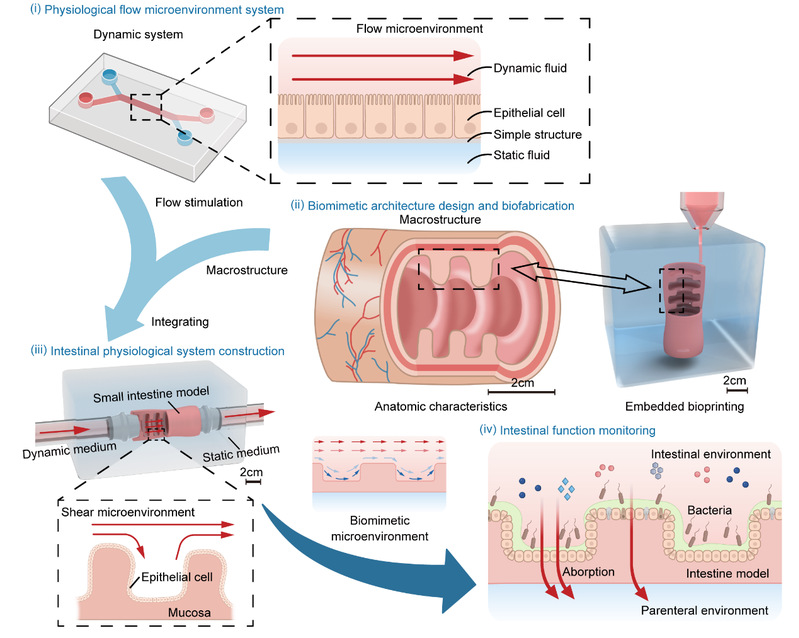
图1 仿生小肠组织构建示意图
01
小肠中的力学密码
小肠中存在消化液、食物残渣的流动,这种流动所产生的剪切力,作为关键信号可以调控肠上皮细胞的两种主要功能——吸收功能和屏障功能。受到稳定剪切力刺激时,细胞会展现出精妙的分工调整——趋向屏障功能主导、吸收功能相对减弱,这一现象与已报道的人体肠道流体力学规律一致(图2)。
更关键的是,这种调节存在开关阈值:当剪切力太弱时,功能变化则不敏感。于是,一个根本性问题浮现出来:人体小肠内各处是否为一致的流动状态?剪切力又是否对小肠不同区域具有相同的调节作用?答案是否定的,由于肠道内关键结构——环形襞的存在(图3)。
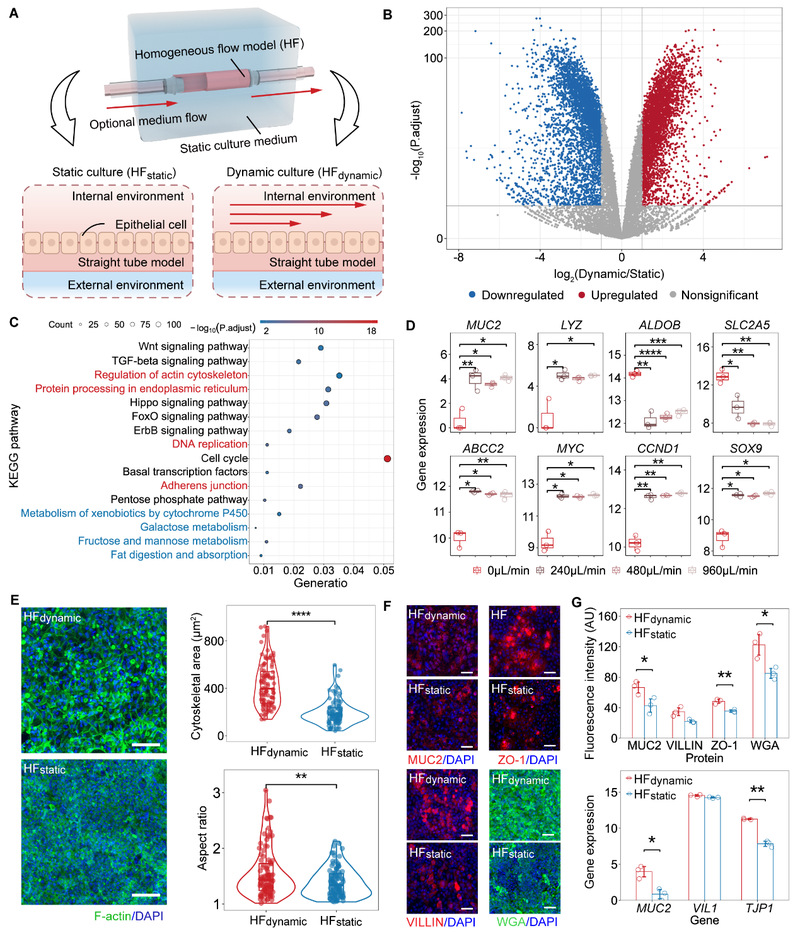
图2 剪切力的功能调控作用
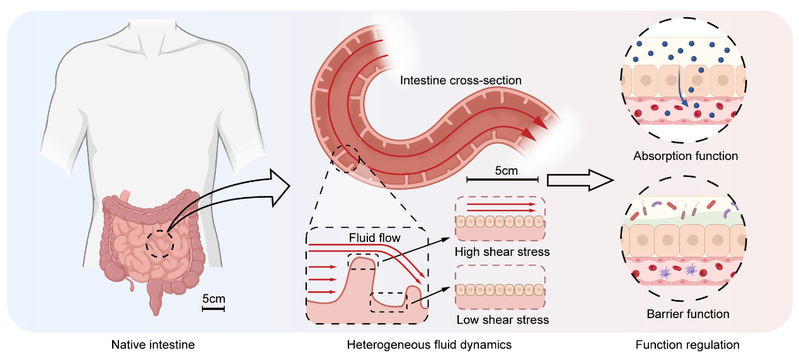
图3 人体小肠中流动分布示意图
02
3D打印小肠结构
小肠内壁的环形褶皱结构影响液体流动过程,它像墙壁一样诱导液体转向,局部改变通道截面与流线分布,改变了流动均一性,使流动状态/剪切力分布更复杂,由此形成独特的肠道功能。
受此启发,团队提出了全新思路:既然结构决定力学环境,力学环境决定功能,那就先通过高精度3D打印,把小肠的环形襞结构造出来。基于天然环形襞的特征设计模型尺寸,并采用水凝胶软材料作为结构基质,通过三维悬浮打印技术实现高精度体外制造。体外模型中流动的可视化结果显示三维流动环境,形成与人体小肠内相似的剪切力分布,成功模拟了天然力学微环境(图4)。
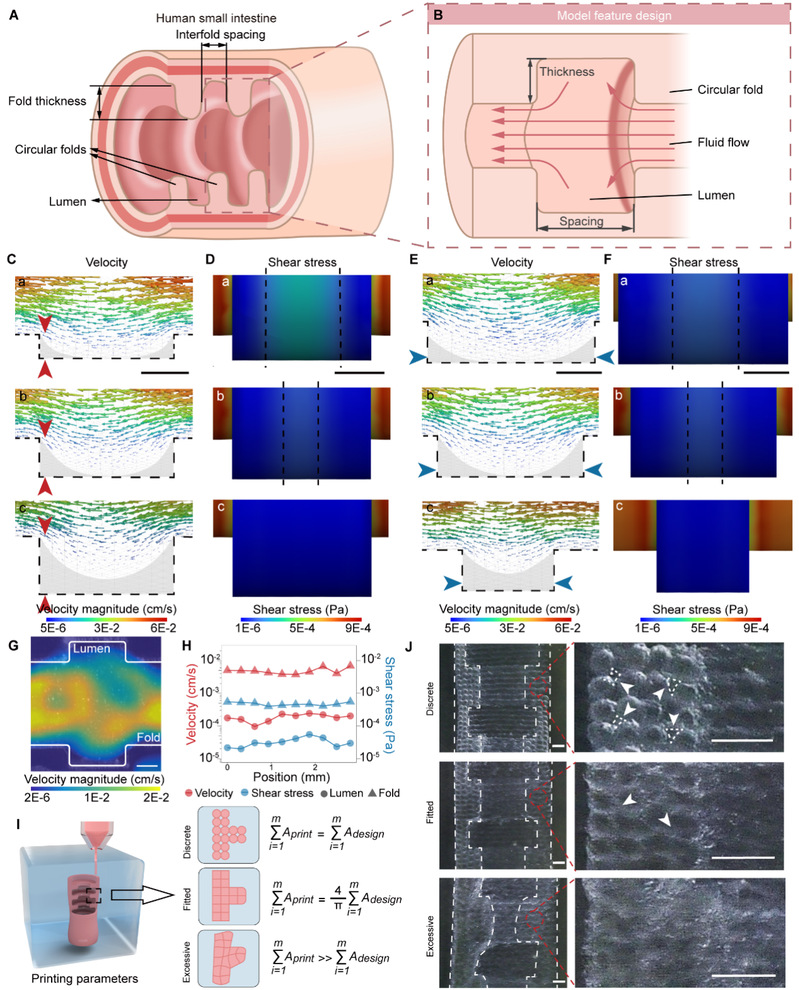
图4 3D打印制造体外小肠组织
03
力学环境调控肠道功能
在完成“结构决定力学环境”这一条件下,团队还要回答一个更重要的问题—力学环境如何决定功能。
仿生的力学环境表现为环形襞区域具有高于“力学开关阈值”的剪切力,而管腔区域具有低于“力学开关阈值”的剪切力,两个区域在剪切力作用下具有显著不同的吸收和屏障功能。特别的是,在环形襞和管腔的过渡区因流场梯度,形成了介于两者之间的功能特征,高度还原了肠道功能的复杂性,由此凸显了局部机械信号在细胞功能特化中的关键作用,更进一步证明了仿生拓扑结构的必要性,真正做到了由“形似”向“神似”的转变(图5)。
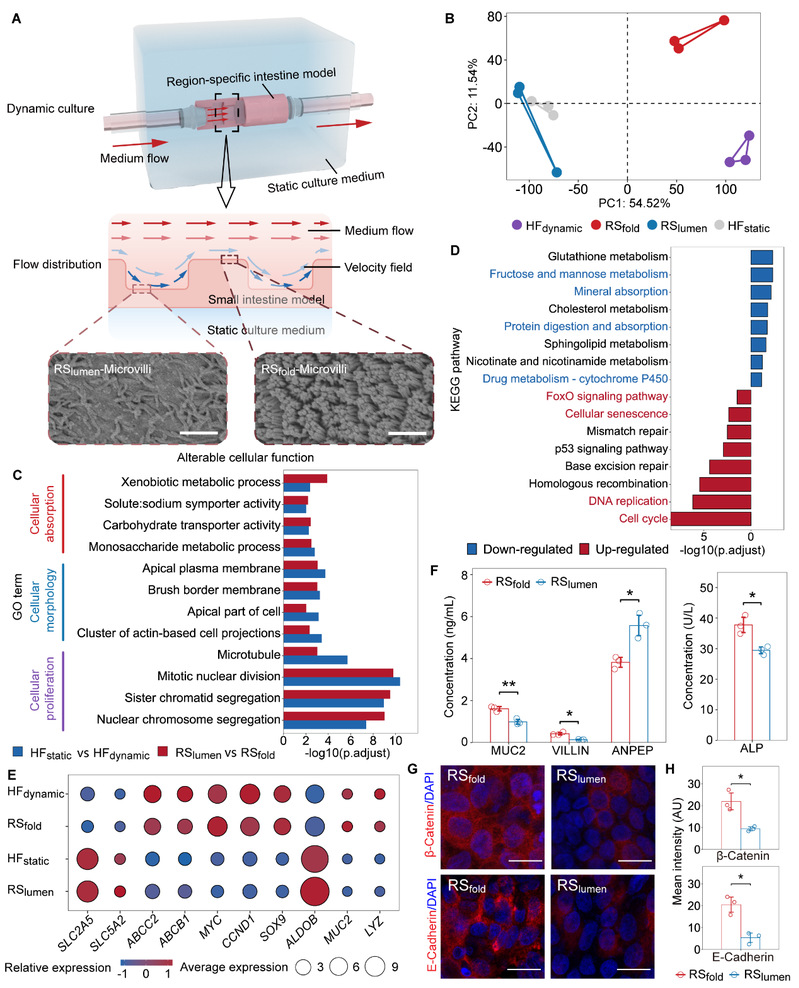
图5 仿生力学微环境还原小肠功能
04
从菌群互作到药物筛选
团队构建的高仿生的人工小肠组织,不仅是结构像、功能像,更在两大前沿领域展现出潜力:
宿主-微生物互作研究:通过流动驱动的力学微环境,可以调控微生物的定植密度,诱导细胞区域特异性的免疫相关分子表达变化和功能重构,还原宿主-微生物相互作用的空间复杂性(图6)。
药物吸收预测:该体系能精准还原仿生吸收功能,完整重现体内复杂的物质吸收过程,实现药物吸收预测的高精度(误差<15%),为个性化药物开发提供了强大平台(图7)。
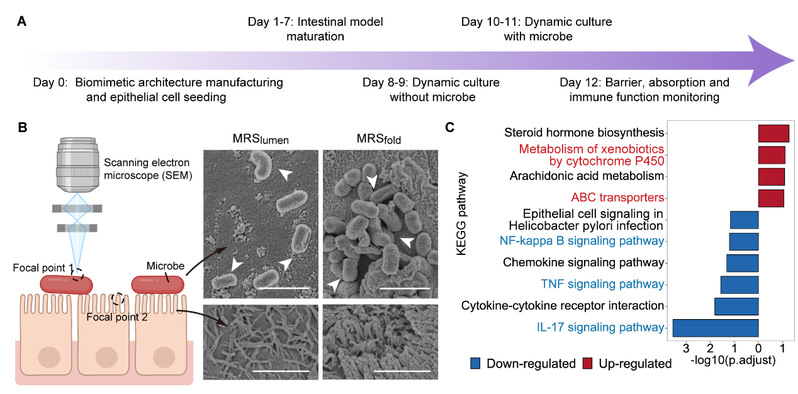
图6 宿主-微生物相互作用研究
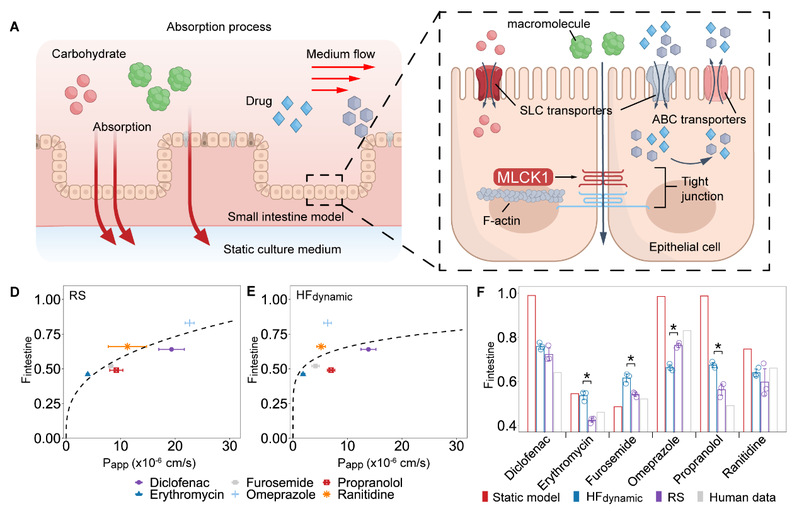
图7 药物吸收预测研究
05
总结
本研究的核心创新体现在一种以工程结构设计为起点、以生理功能还原为目标的体外小肠构建思路。
首先,研究通过仿生小肠宏观几何结构,特别是环形襞等关键形态特征的精确构建,主动塑造了具有生理相关性的力学微环境,使流动与结构之间的相互作用得以自然形成。
其次,在结构—力学耦合框架下,模型同步再现了小肠多项关键功能,包括上皮屏障调控、吸收行为以及与微生物相关的免疫响应,在体外系统复现功能完整性与区域特异性。
进一步地,该模型为复杂生物过程的体外研究提供了高度仿真的实验平台,在微生物定植规律解析、药物与营养物质转运评估以及疾病相关功能研究等方面展现出明确的应用潜力。
总之,这项研究提出了一种全新的体外小肠组织工程设计理念:由拓扑结构定义力学环境,由力学环境调控生理功能, 从而使体外小肠模型从“被动模拟”迈向“功能涌现”,也在体外构建真正具有人体相关性的肠道系统上迈出了关键一步。

